
Рис. 1. Автоматизированный поляризационный сенсор для считывания информации с ДНК-чипов на основе стеклянных призм.
Fig. 1. Automatic polarization sensor for reading information from DNA chips on glass prizm.
Координатор: акад. Власов В. В.
Исполнители: НИБХ, КТИПМ, ИАиЭ, ИХХТ, ИХТТМ СО РАН
C целью разработки новых технологий, методов и приборов для медицинской практики и биологических работ проведены фундаментальные исследования, касающиеся процессов молекулярной гибридизации.
Разработаны оригинальные подходы к получению ДНК-чипов с использованием различных материалов — стекла, мелкодисперсных полимеров, капроновых мембран.
Разработан автоматизированный поляризационный сенсор для считывания информации с ДНК-чипов на основе стеклянных призм (рис. 1). С помощью сенсора можно измерять рефрактометрические характеристики и толщину пленки, изменяющиеся в процессе адсорбции комплементарной цепи ДНК на поверхности призмы, содержащей олигонуклеотидный зонд. Прибор демонстрировался в экспозиции СО РАН на выставке ВТ-2002 оборонного комплекса, г. Москва.
 |
Рис. 1. Автоматизированный поляризационный сенсор для считывания информации с ДНК-чипов на основе стеклянных призм. Fig. 1. Automatic polarization sensor for reading information from DNA chips on glass prizm. |
С целью создания аффинных сорбентов на магнитных носителях осуществлен поиск методов выделения магнитных микросфер из зол основных энергетических углей и методов нанесения белых отражающих покрытий на высокодисперсные порошки ферромагнитных металлов — железа, кобальта и никеля.
Базируясь на результатах фундаментальных исследований высокоселективного лигирования тандема производных трех коротких олигонуклеотидов на матричных ДНК, разработаны высокочувствительные диагностикумы для изучения однонуклеотидного полиморфизма в Y-хромосоме человека, точечной мутации R408W в гене фенилаланин гидроксилазы человека (мутация, характерная при фенилкетонурии) (рис. 2), а также для выявления мутаций в геноме ВИЧ-1, обусловливающих его устойчивость к азидотимидину.
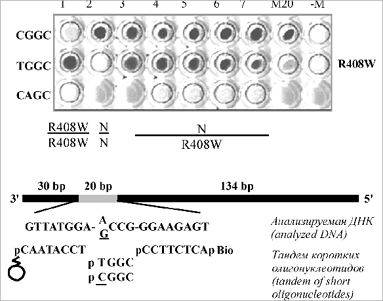 |
Рис. 2. Выявление мутации R408W в образцах ДНК (184 п.о.): Fig. 2. Revealing mutation R408W in DNA samples (184 bp): |
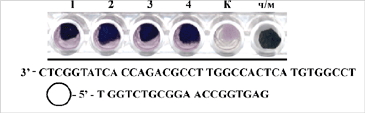 |
Рис. 3. Выявление вируса гепатита С. Fig. 3. Revealing Hepatite C virus: |
Для создания высокоселективных олигонуклеотидных зондов разработана новая эффективная технология выравнивания стабильности комплементарных ДНК—ДНК-комплексов с разным содержанием пар GC и AT, в основе которой лежит использование химерных “мостиковых” олигонуклеотидов, отличающихся от природных олигонуклеотидов наличием в них ненуклеотидных вставок-мостиков. Показано, что созданные химерные олигонуклеотиды, в отличие от природных олигонуклеотидов, способны надежно дискриминировать ДНК, структура которых отличается всего одним нуклеотидным основанием.
С использованием разработанных высокоселективных зондов, иммобилизованных на мелкодисперсный полимер, разработан подход к колориметрическому выявлению и генотипированию широко распространенного вируса гепатита С.
Работа по развитию и внедрению в медицинскую практику метода анализа и генотипирования вируса гепатита С получила поддержку инновационным грантом РФФИ.
Список основных публикаций
 Оглавление Оглавление |
Далее 
|